舟山病理切片免疫组化
免疫组化的结果判断标准主要涵盖:1、患者基本信息,如姓名、年龄、性别和检查时间,这些信息是判断结果准确性的基础;2、病理图像直观展示病变性质,病理诊断结果明确病变类型和原发部位;3、免疫组化指标是关键,常用英文缩写表示,如CEA、NSE、AFP等。阳性表示相应抗原表达,且“+”越多表达性越高。不同指标有不同意义;4、综合分析是主要,医生需结合患者情况、病理图像、诊断结果和免疫组化指标,并参考其他检查结果和临床表现,进行综合判断。免疫组化如何实现对特定蛋白质的高特异性识别?舟山病理切片免疫组化
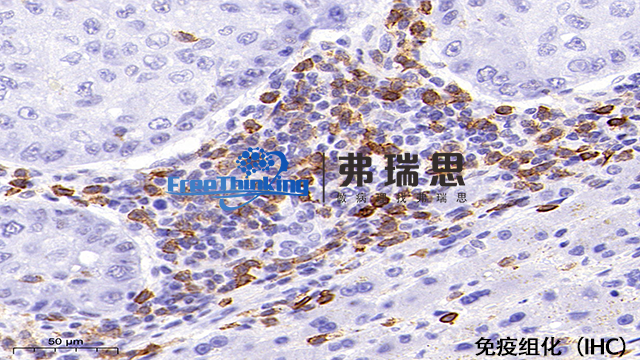
提高免疫组化实验信噪比,确保结果准确,需采取以下策略:1. 精选抗体与滴定:选用高特异性抗体,通过预实验确定有效浓度。2. 封闭:用5%血清或BSA封闭,减少非特异性结合。3. 强化洗涤:每步后充分洗涤,减少残留。4. 优化修复:依据抗原特性调整修复条件,避免过度。5. 抑制内源酶:用过氧化氢处理,控制背景。6. 调控孵育:适当温度和时间孵育抗体,防非特异性结合。7. 精确显色:密切监控显色过程,避免过显。8. 减少荧光干扰:选用特异荧光标记,采用淬灭剂或光谱分离。9. 材料与无菌操作:确保试剂新鲜,操作无污染。10. 对照设置:设立阴性和阳性对照,验证特异性。11. 样本标准化处理:规范固定、脱蜡等,保持样本质量。综合运用这些策略,针对具体条件调整,持续优化实验流程,可明显提升实验质量和可靠性。杭州病理切片免疫组化通过免疫组化可检测特定蛋白的表达情况。
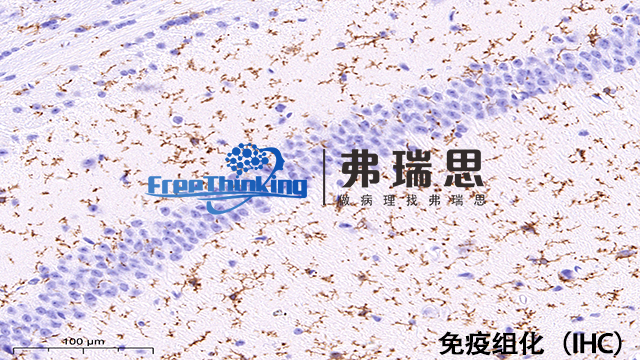
评估免疫组化抗体时,除特异性和敏感性外,还需关注多方面指标:1、稳定性:跨批次及储存期间稳定性确保结果重现性;2、适用性:适配样本类型(如石蜡切片、冷冻切片)及特定染色流程;3、工作浓度:优化浓度以保证结果准确性;4、背景信号:低背景提升结果清晰度;5、交叉反应性:评估非目标抗原反应,尤其多物种研究中;6、线性范围:对定量分析,需保持不同浓度下线性反应;7、可重复性:不同条件下抗体表现一致性是可靠性指标;8、抗体类型:单/多克隆抗体各有千秋,前者特异性强,后者多表位识别增敏;9、验证数据:充足文献或厂家验证,涵盖多样本类型;10、成本效益:平衡价格、效价及实验成功率,选择性价比高的抗体。准确考量这些指标,有助于科研和病理学界选出适宜的免疫组化抗体。
优化多重免疫组化背景高问题策略有以下几点:1、优化封闭,使用血清或BSA预处理减少非特异结合。2、调整抗体浓度,通过滴定找浓度。3、缩短孵育时长和调低温度。4、改善洗涤流程,加强去除未结合抗体。5、选择高特异抗体,减少交叉反应。6、调整抗原修复条件,平衡暴露抗原与背景控制。7、选光谱分离好的荧光染料,用光谱成像减少串色。8、采用TSA等信号放大技术,增强特异信号。9、控制实验条件一致性。10、实施阴性对照,确保结果特异性。免疫组化可帮助评估Tumor的恶性程度。
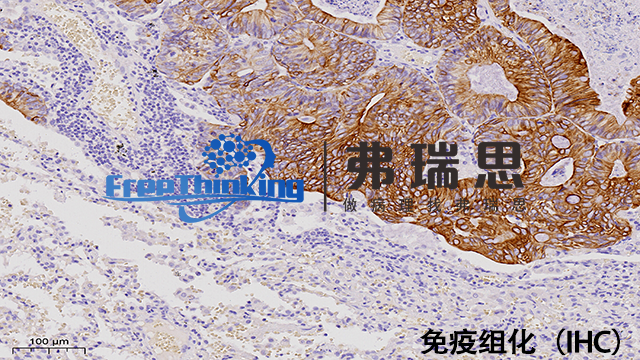
几种常用免疫组织化学方法的原理:1、免疫荧光方法:利用抗原抗体特异性结合的原理,先将已知抗体标上荧光素,以此作为探针检查细胞或组织内的相应抗原,在荧光显微镜下观察。当抗原抗体复合物中的荧光素受激发光的照射后即会发出一定波长的荧光,从而可确定组织中某种抗原的定位,进而还可进行定量分析。2、免疫酶标方法:基本原理是先以酶标记的抗体与组织或细胞作用,然后加入酶的底物,生成有色的不溶性产物或具有一定电子密度的颗粒,通过光镜或电镜,对细胞表面和细胞内的各种抗原成分进行定位研究。免疫酶标技术是目前常用的技术。3、免疫胶体金技术:免疫胶体金技术是以胶体金这样一种特殊的金属颗粒作为标记物。胶体金是指金的水溶胶,它能迅速而稳定地吸附蛋白,对蛋白的生物学活性则没有明显的影响。因此,用胶体金标记一抗、二抗或其他能特异性结合免疫球蛋白的分子(如葡萄球菌A蛋白)等作为探针,就能对组织或细胞内的抗原进行定性、定位,甚至定量研究。在Tumor研究中,免疫组化是鉴定Tumor标志物、了解其表达模式的关键工具。扬州病理切片免疫组化扫描
多重免疫组化技术可同时检测多种蛋白质,为复杂疾病机制研究打开新视角。舟山病理切片免疫组化
确保跨实验室免疫组化(IHC)结果可比性,是保障科研及临床准确性的关键。以下是关键标准化策略:1、抗体标准:选用高特异、敏感且经多实验室验证的商业化抗体,记录抗体详细信息,保证批次稳定性。2、统一抗原修复:各实验室采用相同或根据抗体优化的抗原修复条件,减少变异性。3、标准化流程:制定详尽操作规程,涵盖从样本处理到结果分析的全过程,确保操作一致性。4、设立对照:每项实验含阳/阴性及内参对照,确保实验有效性和结果比对性。5、染色强度标准化评估:采用统一评分系统(H-score等),减少主观性。6、参与质控:加入国际或国内EQA计划,或定期与参考实验室比对,监控检测性能。7、仪器校准:定期校准检测设备,维持性能稳定,减小设备差异影响。8、数据管理:标准化数据记录与分析流程,统一软件算法,确保分析连贯可追溯。9、人员培训:定期培训,提升操作技能,降低人为误差。10、持续改进:建立反馈机制,分析差异原因,不断优化流程,追求持续质量提升。舟山病理切片免疫组化
上一篇: 常州多重免疫组化
下一篇: 连云港多色免疫荧光病理染色实验流程