带培养基拭子管采购信息
无菌拭子管(带培养基的无菌取样棉签)主要应用于填充针、设备凹槽、不平整表面和洁净室或隔离器中的管道表面擦拭取样。采样区域:可擦拭25平方厘米产品信息:定量测试的无菌拭子管(液体成分:含有卵磷脂+吐温80中和剂的缓冲溶液):货号拭子材质液体容量包装形式备注信息S31Q聚酯纤维10毫升1支/包5包/袋40袋/箱(200支)洗脱后经薄膜过滤后计数S32Q植绒纤维0.1毫升直接涂布到TSA平皿上计数用于定性测试的无菌拭子管(液体成分:含有卵磷脂+吐温80中和剂的TSB溶液)洁净区用无菌拭子管购买,请联系上海荣熠生物科技。带培养基拭子管采购信息
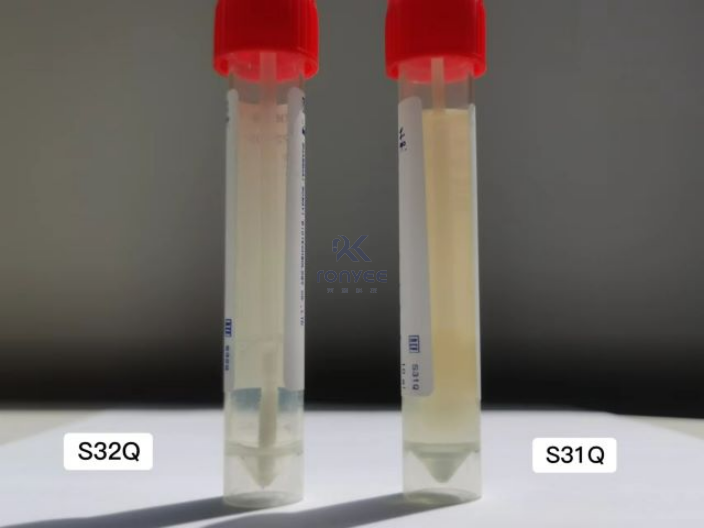
在日常的环境监测中,接触碟法和棉签擦拭法是对药品无菌生产进行表面微生物监测的常用方法。
无菌拭子管(带培养基的无菌取样棉签)主要应用于填充针、设备凹槽、不平整表面和洁净室或隔离器中的管道表面擦拭取样。
定量分析:
定量测试的无菌拭子管(液体成分:含有卵磷脂+吐温80中和剂的缓冲溶液):
|
货号 |
拭子材质 |
液体容量 |
包装形式 |
备注信息 |
|
S31Q |
聚酯纤维 |
10毫升 |
1支/包 5包/袋 40袋/箱(200支) |
洗脱后经薄膜过滤后计数 |
|
S32Q |
植绒纤维 |
0.1毫升 |
直接涂布到TSA平皿上计数 |
定性分析:
定性测试的无菌拭子管(液体成分:含有卵磷脂+吐温80中和剂的TSB溶液)
|
货号 |
拭子材质 |
液体容量 |
包装形式 |
备注信息 |
|
S31N |
聚酯纤维 |
10毫升 |
1支/包 5包/袋 40袋/箱(200支) |
直接培养观察液体浑浊情况 |
|
S32N |
植绒纤维 |
10毫升 |
用于无菌隔离器或者RABS系统的无菌拭子管套管:
|
货号 |
拭子材质 |
液体容量 |
包装形式 |
备注信息 |
|
S31I |
聚酯纤维 |
5mL(无菌水)+5mL(TSB溶液) |
2支/包 3包/袋 40袋/箱(120套) |
直接培养观察液体浑浊 |
|
S32I |
植绒纤维 |
5mL(无菌水)+5mL(TSB溶液) 进口表面擦拭拭子管价位无菌拭子管生产厂家,上海荣熠生物科技。 |
采样区域:
可擦拭25平方厘米
药品生产质量管理规范(2010年)附录1无菌药品第十一条“应当对微生物进行动态监测,评估无菌生产的微生物状况。监测方法有沉降菌法、定量空气浮游菌采样法和表面取样法(如棉签擦拭法和接触碟法)等在日常的环境监测中,接触碟法和棉签擦拭法是对药品无菌生产进行表面微生物监测的常用方法。无菌拭子管(带培养基的无菌取样棉签)主要应用于填充针、设备凹槽、不平整表面和洁净室或隔离器中的管道表面擦拭取样。定量分析:定量测试的无菌拭子管(液体成分:含有卵磷脂+吐温80中和剂的缓冲溶液):货号拭子材质液体容量包装形式备注信息S31Q聚酯纤维10毫升1支/包5包/袋40袋/箱(200支)洗脱后经薄膜过滤后计数S32Q植绒纤维0.1毫升直接涂布到TSA平皿上计数采样区域:可擦拭25平方厘米擦拭方法:将拭子管以30°角度与取样表面接触,缓慢并充分擦拭。在向前移动的同时将其从一边移到另一边,擦拭过程覆盖整个涂布区域。然后翻转拭子,让拭子的另一边也进行擦拭,擦拭方向与前一次擦拭移动方向垂直(注意:每次取样尽可能采用相同的力度、擦拭速度、以及擦拭路径。)带培养的无菌取样棉签使用方法。
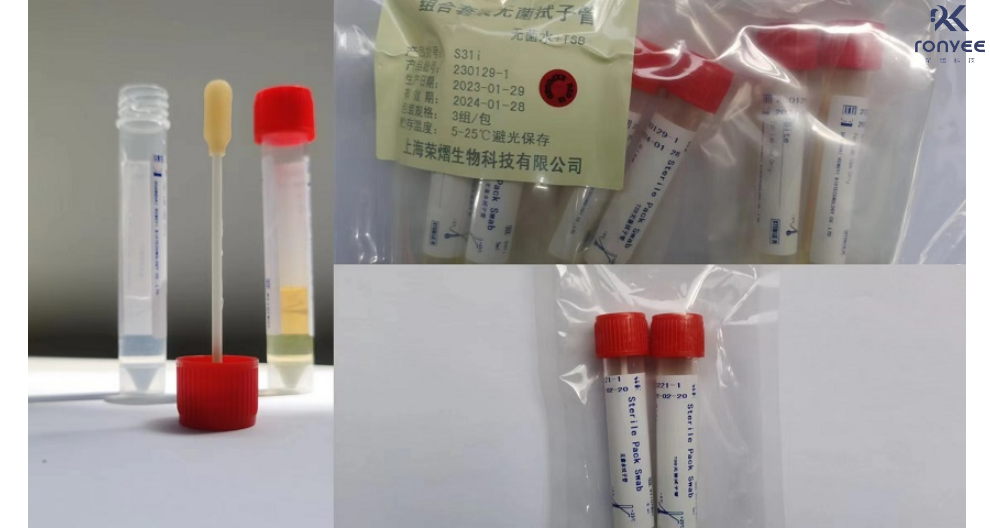
无菌取样棉签宽头可折断设计,无菌单支包装,适用清洁验证的擦拭取样。产品优势:无菌包装:无菌单支包装,伽马射线辐照灭菌,随货提供COA质量报告耐磨实用:无尘布头热封边紧紧锁死切边,有效防止微尘粒产生,无尘布具有优越的耐磨性和洁净性能柔软光滑:做工精细,棉签表面柔软圆滑,细腻不伤物品清洁力佳:做工标准,清洁强,可反复擦拭可折断设计:柄身采用聚丙烯材质,可折断设计订货信息:货号S821名称无菌擦拭棉签规格1支/1内包,50支/1大包表面微生物取样的回收率怎么计算?聚酯纤维拭子管采购信息
无菌拭子管取样后直接培养嘛?带培养基拭子管采购信息
清洗验证的定义
有文件和记录证明所批准的清洁规程能有效地清洁设备,使之符合药品生产要求.
2010 年版 GMP 正文:
一百四十三条清洁方法应当经过验证,证实其清洁的效果,以有效防止污染和交叉污染。清洁验证应当综合考虑设备使用情况、所使用的清洁剂和消毒剂、取样方法和位置以及相应的取样回收率、残留物的性质和限度、残留物检验方法的灵敏度等因素。
清洗验证的法规与指南
FDA(cGMP):21CFR-PARTS 210 & 211 211.67
设备清洁与维护
间隔一定时间应该对设备和用具进行清洗、维护和消毒,防止可能的故障和污染及改变药品安全性、均一性、效价、质量和纯度。
EU GMP:
336 生产设备的设计必须容易进行彻底清洁,必须按照详细的书面操作规程进行清洁并储存在清洁干燥的条件下。
337 洗涤和清洁设备必须正确选择,保证在使用时不会带来污染。
WHO-937-附录 3:清洁验证 1.4 清洁验证
目的在于证明设备始终符合产品、清洗剂和微生物残留验收要求,以预防可能的污染和交叉污染。
指南:ICH Q7FDA《清洁验证检查指南》Ø
批准/受控的清洗程序Ø验证方案
Ø经过验证的化学/微生物检测方法
Ø批准的验证报告(结论:清洁程序
有效,达到可接受标准)
Ø有效的培训/变更控制
清洗验证的要求GMP的要求
带培养基拭子管采购信息
上一篇: 进口带培养基拭子棉签使用方式
下一篇: 小于10ppb TOC取样瓶推荐厂家